Insuficiência Venosa
Insuficiência Venosa

A Insuficiência Venosa Crónica (IVC) é uma condição em que as veias das pernas apresentam dificuldade em transportar o sangue de volta ao coração. Em condições normais, as veias possuem válvulas que impedem o sangue de retroceder por ação da gravidade. Quando estas válvulas não funcionam corretamente ou as paredes das veias estão enfraquecidas, o sangue acumula-se nas pernas, causando o que chamamos de estase venosa.
Sintomas
Os sintomas tendem a agravar-se ao final do dia ou após longos períodos de pé ou sentado:
-
Sensação de peso e cansaço: Frequentemente descrita como “pernas pesadas”.
-
Edema (Inchaço): Localizado principalmente nos tornozelos e pés.
-
Varizes: Veias dilatadas, tortuosas e visíveis sob a pele.
-
Alterações na pele: Escurecimento (pigmentação ocre), pele seca ou avermelhada.
-
Cãibras e formigueiro: Especialmente durante a noite.
-
Úlceras venosas: Em estágios avançados, podem surgir feridas de difícil cicatrização junto ao tornozelo.
Causas
A insuficiência venosa resulta do aumento da pressão sanguínea nas veias por tempo prolongado:
-
Disfunção Valvular: Válvulas que não fecham totalmente.
-
Sedentarismo: A falta de contração dos músculos da barriga da perna (a “bomba muscular”) dificulta o retorno do sangue.
-
Histórico Familiar: Genética é um fator preponderante.
-
Idade e Género: Mais comum em mulheres e em idades avançadas.
-
Fatores Hormonais: Gravidez e uso de contracetivos.
-
Obesidade: O excesso de peso aumenta a pressão intra-abdominal e venosa.
Diagnóstico
O diagnóstico é clínico, mas complementado por exames que avaliam o fluxo sanguíneo:
-
Exame Físico: Observação de varizes, edema e alterações tróficas da pele.
-
Eco-Doppler Venoso: O exame de eleição. Utiliza ultrassons para visualizar as veias e detetar se o sangue está a fluir no sentido errado (refluxo).
-
Pletismografia: Avalia as mudanças de volume na perna para medir a eficiência do retorno venoso.
Tratamento (Médico e Fisioterapêutico)
O tratamento foca-se em melhorar a circulação e reduzir a pressão venosa.
Intervenção Médica:
-
Terapia de Compressão: Uso de meias de compressão elástica (essencial para “apertar” as veias e ajudar as válvulas).
-
Medicação Venotónica: Fármacos que ajudam a aumentar o tónus das paredes venosas.
-
Escleroterapia ou Cirurgia: Procedimentos para fechar ou remover veias gravemente danificadas (varizes).
Intervenção da Fisioterapia:
-
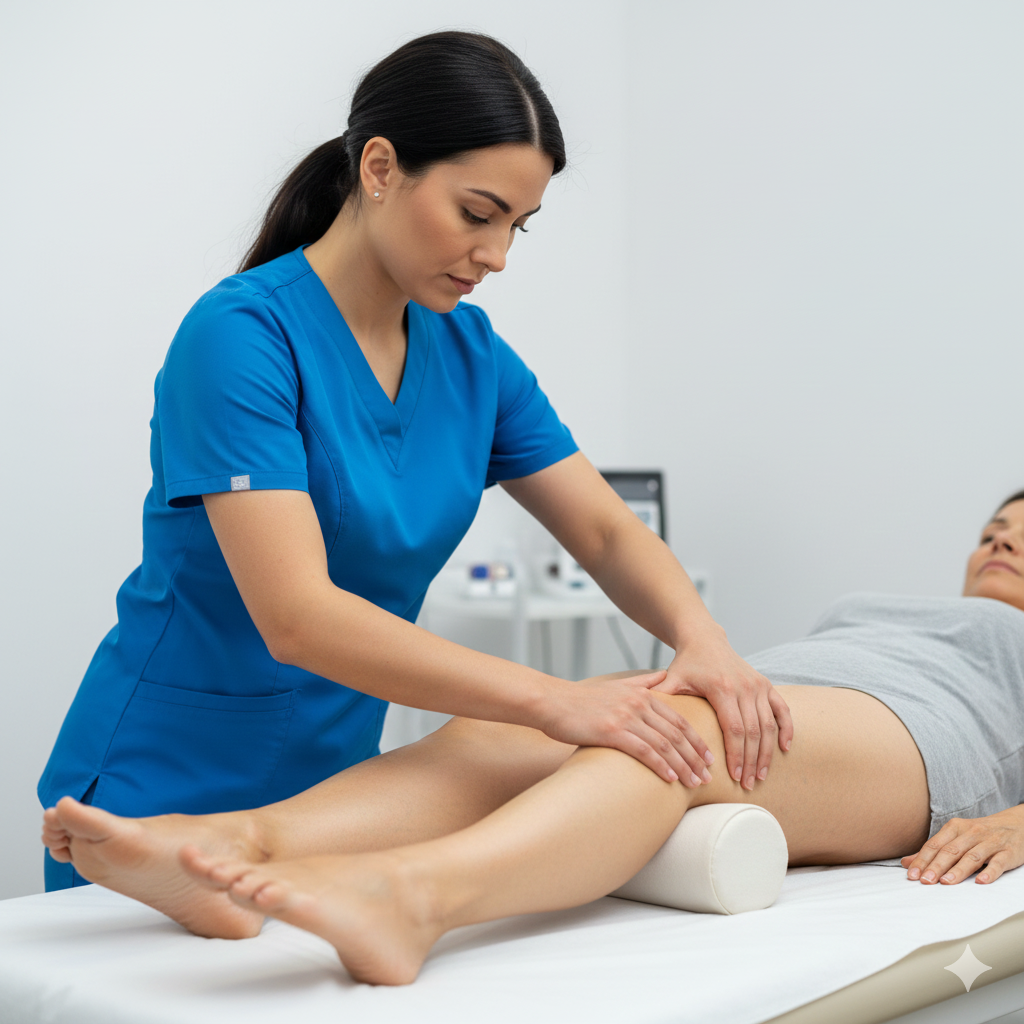
Drenagem Linfática Manual (DLM): Técnica de massagem suave e rítmica que ajuda a deslocar o excesso de líquido acumulado nos tecidos de volta para a circulação.
-
Pressoterapia: Uso de aparelhos que exercem compressão pneumática intermitente, simulando uma massagem compressiva.
-
Exercícios de Bomba Muscular: Fortalecimento dos músculos gémeos (panturrilha). Como o músculo é o “coração das pernas”, a sua contração é o que mais ajuda o sangue a subir.
-
Cinesioterapia Vascular: Exercícios específicos realizados com as pernas elevadas (como movimentos de pedalagem ou flexão do tornozelo).
-
Cuidados Posturais: Reeducação para evitar períodos prolongados de imobilidade e ensinar o posicionamento de elevação dos membros durante o repouso.
Prevenção
-
Atividade Física: Caminhar regularmente é a melhor forma de manter a bomba muscular ativa.
-
Elevação das Pernas: Repousar com os pés acima do nível do coração por 15-20 minutos diários.
-
Controlo de Peso: Reduzir a carga sobre o sistema circulatório.
-
Evitar Calor Excessivo: Depilação a cera quente, saunas ou exposição solar prolongada dilatam as veias e agravam o quadro.
-
Hidratação da Pele: Manter a pele das pernas hidratada para evitar fissuras e infeções.